En esta entrada del blog vamos a continuar con la introducción sobre el verraco, hoy toca hablar de la fisiología. Para ello nos centraremos en la espermatogénesis y su control hormonal. Proceso mediante el cual se forman las células espermáticas.
La espermatogénesis ocurre de manera centrípeta en los túbulos seminales, comprendiendo el conjunto de etapas que transcurren hasta que finalmente una célula germinal se convierte en un espermatozoide. Este proceso se desarrolla completamente en los testículos y está modulado hormonalmente de manera central, mediante el eje hipotálamo-hipofisis-gonadal. El sistema neuroendocrino es el responsable de su control y la función de los órganos reproductivos mediante regulación hormonal. Está constituido por el sistema nervioso que lleva los impulsos hasta el hipotálamo y por el sistema endocrino, la hipófisis, que liberara las hormonas que actuarán de manera periférica.
El hipotálamo, va a ser el encargado de interactuar con el sistema nervioso y endocrino. El eje hipotálamo hipofisario transporta las hormonas hipotalámicas a la hipófisis vía vascular de manera directa. Estas hormonas hipotalámicas (GnRH) van a ser secretadas a partir de cierta información percibida por los órganos sensoriales. La hipófisis realizará la función regulatoria endocrina, ya que es la encargada de producir las hormonas (LH y FSH) que tendrán un efecto directo en tejidos diana, en este caso los testículos. A su vez tanto el hipotálamo como la hipófisis son órganos diana de otras hormonas producidas periféricamente (testosterona e inhibina), de esta manera se conforma un sistema de retroalimentación que se autorregula por si solo, ya que las hormonas secretadas desde las gonadas llegarán hasta la hipófisis deteniendo la producción de gonadotropinas. Estos circuitos, van a estar condicionados por aspectos como la edad (maduración sexual del macho), fotoperiodo e intensidad lumínica e incluso la alimentación, entre otros.
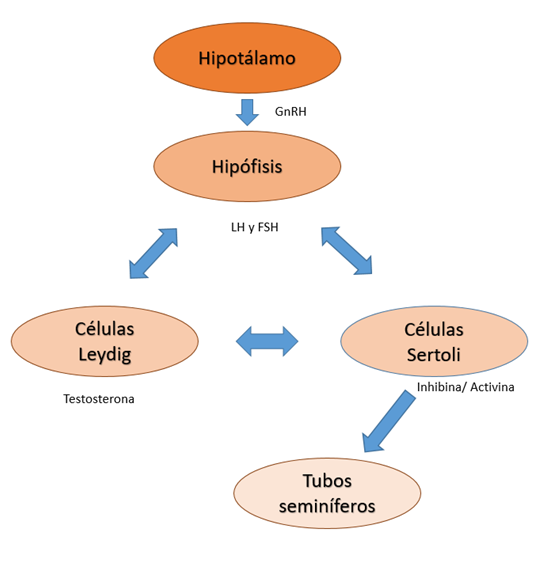
Imagen 1: esquema eje hipotálamo hipofisario gonadal.
Fuente: Adaptado de Philippe Le Coz, Anatomia y Fisiología del Verraco. (2006)
Durante el crecimiento del futuro reproductor, las hormonas gonadotropinas tienen diferentes funciones, por ejemplo, la FSH es la responsable de la proliferación de las células de Sertoli que están ubicadas en los túbulos seminíferos durante el periodo postnatal, estableciendo su número total antes del periodo prepuberal. Esto determinará el tamaño testicular y por tanto la producción de espermatozoides de cada individuo, una vez el verraco sea sexualmente maduro, ya que las células de Sertoli dan soporte físico y metabólico a las células germinales.
La hormona LH, interviene en la proliferación, hipertrofia y establecimiento de los órganos sexuales, durante la fase de desarrollo. Esta hormona tiene como principal objetivo las células de Leydig, que se encuentran situadas en tejido conectivo circundante a los túbulos seminíferos. Éstas células presentan receptores tanto para la LH como para la FSH. Las células del Leydig al ser activadas por la acción de la LH, producirán testosterona. Esta testosterona es necesaria para mantener las funciones de las células de Sertoli y el correcto desarrollo de la espermatogénesis. Además, la testosterona es esencial a la hora de iniciar la madurez y de los niveles sanguíneos de esta hormona van a depender el desarrollo de los testículos, pubertad, madurez sexual y por último la producción de espermatozoides.
Como comentamos previamente, toda esta regulación hormonal depende de manera central del hipotálamo y la hipófisis, y se autoregula mediante la secreción en las gonadas de inhibina, andrógenos y estrógenos que llegarán hasta la hipófisis regulando la producción de gonadotropinas. De este proceso dependerá completamente la espermatogénesis que se divide en dos partes principales, espermatocitogénesis y espermiogénesis:
La espermatocitogénesis, es la etapa inicial y comienza con las células germinales o espermatogonias. Estas células sufren una expansión drástica tanto en número como en maduración durante los 4-5 meses de edad y una posterior estabilización sobre los 7 meses, es por esto que los sementales no se deben utilizar como tal hasta los 7 meses de edad, aunque esto depende mucho de la raza y línea genética. Esto es importante ya que cada vez se intenta incorporar a producción verracos más jóvenes debido a su mejor genética y esto acaba reflejándose en espermiogramas inmaduros. La espermatocitogénesis comprende las fases entre espermatogonia y espermatida. Las espermatogonias pueden ser:
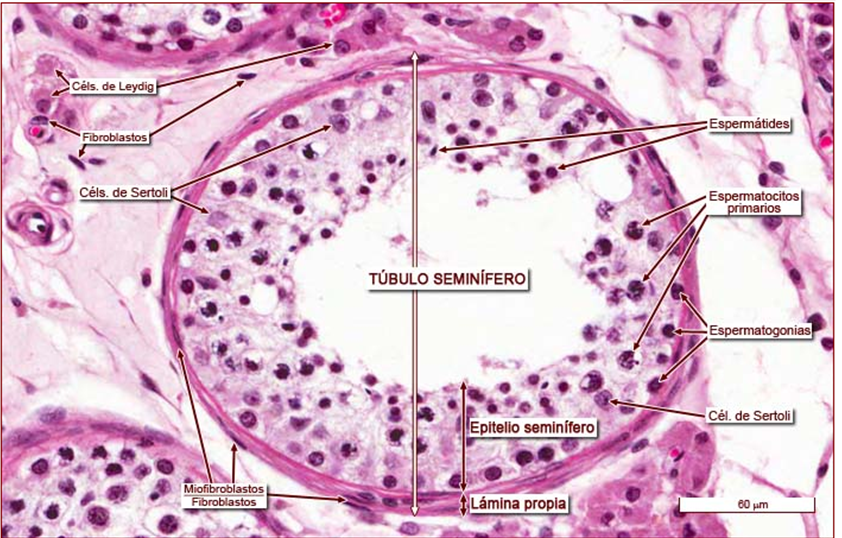
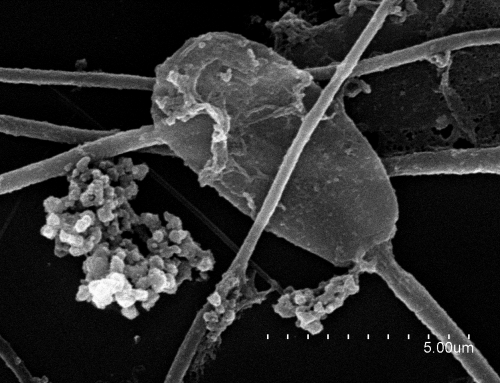
Imagen 2: Túbulo seminífero
Fuente: Universidad de Zaragoza
- Indiferenciadas, o tipo A, cuya función es el mantenimiento del pool de células durante la vida del semental, para ello parte de estas espermatogonias permanecen sin dividirse hasta que se han formado los espermatocitos primarios (fruto de la meiosis) e iniciar otra oleada de divisiones.
- Espermatogonias diferenciadas o A1, A2, A3 y A4, dependiendo de la división celular, el número de divisiones va a depender de la especie animal.
- Espermatogonias tipo B, que son el ultimo tipo celular antes de iniciar la división meiótica.
Mediante mitosis se irán generando en cascada los diferentes tipos de células hasta generar los espermatocitos primario. Los espermatocitos primarios se dividirán mediante meiosis dar lugar a los espermatocitos secundarios, que en una segunda división meiótica se transformarán en espermátidas.
La espermatogénesis culmina con la espermiogénesis que es la fase donde se van a producir cambios en esas espermátidas obtenidas de la espermatocitogénesis hasta llegar a obtener un espermatozoide. Los cambios celulares, se dan principalmente a nivel del núcleo (condensación y reducción de tamaño) y del citoplasma (eliminación de citoplasma y formación del acrosoma y flagelo). Durante este proceso adquieren importancia las células de Sertoli, que se encuentran en el interior de los túbulos seminíferos y presentan receptores de andrógenos y FSH para la mediación del proceso.
Dentro de este proceso encontramos la espermiación, así se denomina al proceso de liberación del espermatozoide de la estructura protectora de las células de Sertoli para salir a los conductos seminíferos pasando por la red de testis y acabar en el epidídimo, donde madurarán a lo largo del cuerpo del epidídimo, quedando almacenados en la cola del mismo.
El objetivo de la maduración es realizar todos los cambios necesarios para dotar a la célula espermática de capacidad de movimiento y fecundación. Estas funciones, son dependientes de andrógenos y estrógenos presentes en los fluidos que acompañarán al espermatozoide. La célula espermática presenta receptores para estas hormonas. Los andrógenos y estrógenos son indispensables para el mantenimiento de la morfología epitelial, dotación de proteínas de unión a la zona pelúcida, adquisición de motilidad y protección de las células durante el almacenamiento en la cola del epidídimo.
Como hemos visto el proceso de la producción seminal es un proceso complejo, hormonalmente regulado y al que puede afectar múltiples factores. La estacionalidad y el fotoperiodo, al igual que las hembras tienen gran importancia, el carácter estacional de la especie porcina en el macho, afecta principalmente al número de espermatozoides por eyaculado. La calidad espermática puede alterarse por la temperatura. El estrés térmico puede ser un gran problema en todos los ámbitos de la producción porcina, este estrés suele afectar disminuyendo la calidad de los espermatozoides. Un déficit en la alimentación también nos podría producir una bajada del rendimiento reproductivo, aunque estaríamos hablando de déficits prolongados en el tiempo, al final, como siempre se ha dicho, la reproducción es una función “de lujo” y que se puede ver afectada rápidamente si las condiciones no son las idóneas. Otros factores que podrían intervenir en la producción espermática es el ritmo de colecta, el desarrollo y maduración óptimo del verraco en su fase de crecimiento entre otras.
Todos estos factores al final van a tener una repercusión en la producción cuantitativa y cualitativa de los espermatozoides, por ello es importante desarrollar estrategias para minimizar el efecto negativo de estos factores y así maximizar la producción seminal en los verracos.
Con estas dos entradas concluye el recordatorio anatomo-fisiológico del verraco. Esperamos que haya servido para asentar los conocimientos y entender un poco mejor cómo funciona el proceso por el cual se producen y maduran las células espermáticas.
BIBLIOGRAFÍA
Bonet, S., Garcia, E., Sepúlveda, L. 2013. The Boar Reproductive System. In: Bonet S., Casas I., Holt W., Yeste M. (eds) Boar Reproduction. Springer, Berlin, Heidelberg.
de Loera Ortega, Y. 2016. Efecto de la fuente y nivel d zinc en el comportamiento productivo de machos no castrados (40-110 kg) y su relación con el comportamiento sexual. Tesis doctoral Universidad Complutense de Madrid, Facultad de veterinaria.
Einarsson S., Andersson K., Wallgren M., Lundström K., Rodriguez-Martinez H. 2009. Short- and long-term effects of immunization against gonadotropin-releasing hormone, using Improvac™, on sexual maturity, reproductive organs and sperm morphology in male pigs. Theriogenology 71 (2); 302–310.
França L.R., Avelar G.F., Almeida F.F. 2005. Spermatogenesis and sperm transit through the epididymis in mammals with emphasis on pigs. Theriogenology, 63(2), 300-318.
Hafez, E.SE. (2000) Reproducción e inseminación artificial en animales. Mc Graw-Hill. México.
Johnson F.O., Gilbreath E.T., Ogden L., Grahamd T.C., Gorham S. 2011. Reproductive and developmental toxicities of Zinc supplemented rats. Reproductive Toxicology 31 (2); 134–143.
Romeo R.D., Richardson H.N., Sisk C.L. 2002. Puberty and the maturation of the male brain and sexual behavior: recasting a behavioral potential. Neuroscience & Biobehavioral Reviews. 26, (3): 381-391.
Úbeda, J.L., Dahmani, Y., Ausejo, R. (Marzo, 2011). Fisiología Reproductiva del Verraco. Suis, 75: 32-41.
https://www.thepigsite.com/genetics-and-reproduction/insemination/anatomy-and-physiology-1
https://www.3tres3.com/articulos/anatomia-y-fisiologia-del-verraco_4025/